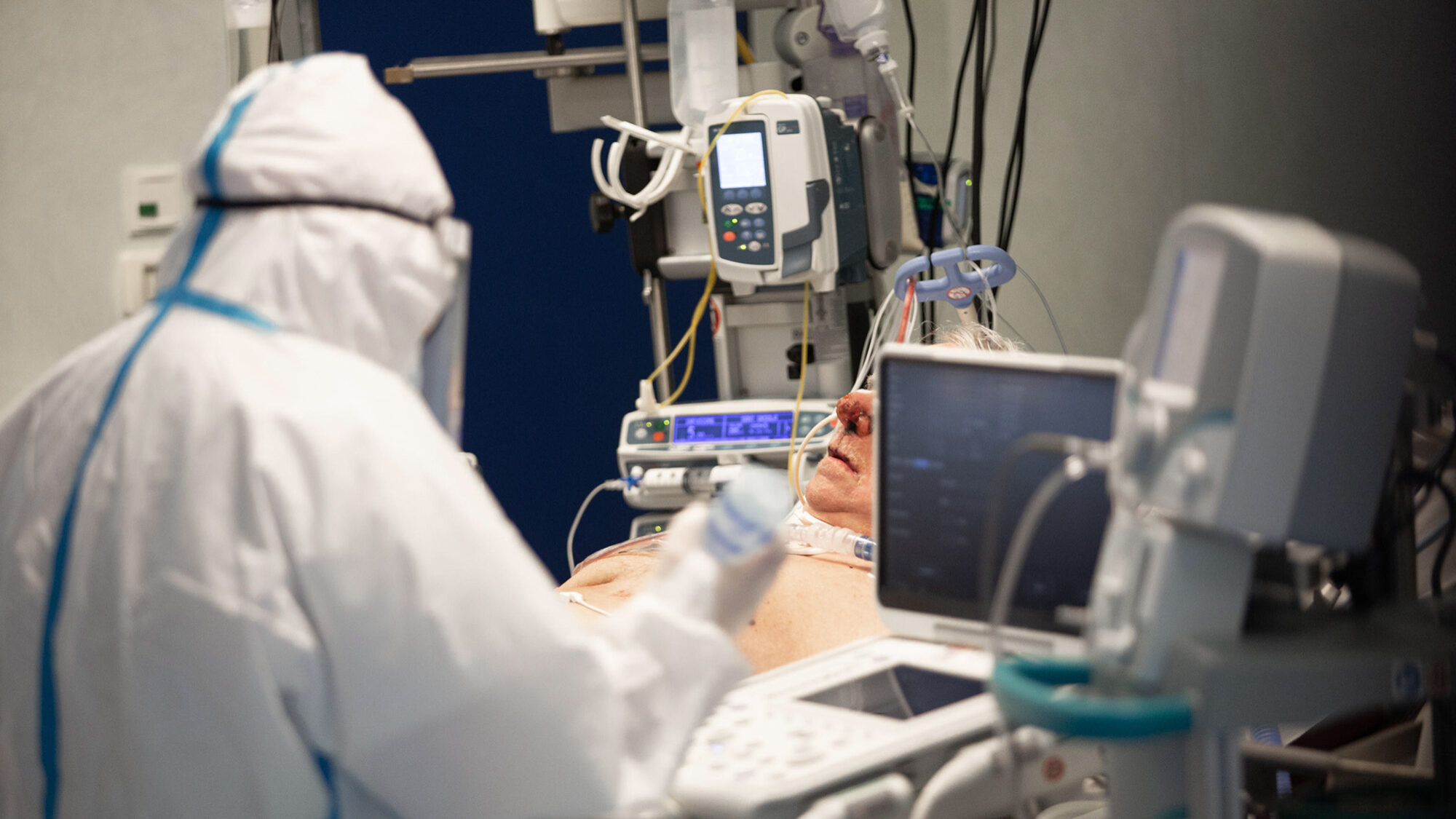
Desenvolvimento de antivirais contra a Covid-19 ainda está em fase embrionária
"EMA está a avaliar os dados sobre quatro tratamentos Covid-19" em processo de avaliação, que recorrem a anticorpos projetados para se ligarem à proteína "spike" do vírus, diz Aranda da Silva.
Ao contrário das vacinas, o rápido desenvolvimento de medicamentos específicos para tratar a Covid-19 não parece tão promissor, apesar de a atenção do regulador europeu estar centrada em seis fármacos à base de antivirais e anticorpos.
“A investigação de um medicamento específico seria a situação ideal, mas estamos ainda longe de o conseguir, mesmo tendo em conta os enormes recursos que estão a ser utilizados, dado estarmos perante uma pandemia com grande impacto económico e social em todos os países”, adianta à Lusa o especialista em indústria farmacêutica José Aranda da Silva.
Para já, a Agência Europeia do Medicamento (EMA, na sigla em inglês) apenas aprovou, em junho de 2020, o antiviral remdesivir para o tratamento da Covid-19 em adultos e adolescentes a partir de 12 anos e com pneumonia, que requerem oxigénio suplementar.
De acordo com a EMA, quatro tratamentos antivirais estão ainda em análise continua pelos especialistas da organização europeia, enquanto outros dois medicamentos imunossupressores já estão na fase mais avançada de avaliação com vista à autorização de comercialização nos países da União Europeia (UE).
“A EMA está, atualmente, a avaliar os dados sobre quatro tratamentos Covid-19″ em processo de avaliação continua, que recorrem a anticorpos projetados para se ligarem à proteína “spike” do vírus, reduzindo a sua capacidade de atingir as células do corpo, adiantou o regulador europeu à Lusa, que garante que o processo decorre “no prazo mínimo necessário” para garantir uma avaliação completa dos riscos e benefícios destes medicamentos.
A revisão continua é uma ferramenta regulatória ao dispor da EMA para acelerar a avaliação de um novo medicamento em situações de emergência de saúde pública, tendo já sido utilizado para a aprovação de comercialização das quatro vacinas contra o vírus SARS-CoV-2 que estão a ser usadas nos países da UE.
Além dos processos de avaliação, o regulador europeu também disponibiliza aconselhamento às empresas e laboratórios farmacêuticos sobre as mais recentes orientações regulamentares e científicas.
Aranda da Silva, primeiro presidente do Autoridade Nacional do Medicamento (Infarmed), salienta que a comunidade científica ainda está a conhecer a forma como o SARS-CoV-2 se comporta no organismo, o que se deve ao facto de o seu genoma ter sido divulgado há pouco mais de um ano.
Além disso, “se analisarmos a disponibilidades de terapêuticas de anti-infecciosos — bactérias e vírus — registamos que, comparativamente com outras patologias, têm sido aprovados poucos medicamentos nos últimos anos. São poucos os antibióticos recentes no mercado. Quanto a antivíricos, ao que me recordo, os últimos, específicos para a hepatite C, foram aprovados há mais de cinco anos“, disse o antigo bastonário da Ordem dos Farmacêuticos.
No desenvolvimento deste tipo de medicamentos “é preciso ter em conta que os vírus são diferentes”, salientou José Aranda da Silva, apontando o exemplo do vírus da sida, para o qual não se conseguiu até agora descobrir uma vacina, uma vez que a “forma como interage como o sistema imunitário tem impedido essa descoberta”.
De acordo com o especialista em regulamentação farmacêutica, a Organização Mundial da Saúde e algumas autoridades reguladoras nacionais desenvolveram também ensaios clínicos com diversos fármacos já conhecidos e que poderiam ser úteis no tratamento da Covid-19, mas os seus resultados “não têm sido muito animadores”.
Perante esse possível impasse, Aranda da Silva defende que, até final deste ano, a questão fundamental passa por reforçar a cobertura vacinal em todos os países, aumentando a produção de vacinas, tendo em conta que “tudo aponta que a imunização provocada não é muito duradoura e a efetividade global (mundo real), como acontece noutras vacinas, poderá ser inferior a 80%”.
O antigo membro da administração da EMA atribuiu também a rapidez com que foram desenvolvidas as vacinas ao facto de já existirem estudos, desde a epidemia de SARS em 2003 e da MERS em 2012, que tentavam encontrar novas plataformas para a sua produção, assim como ao “enorme investimento” público nos Estados Unidos e na Europa que permitiu acelerar o processo.
“O terceiro fator foi a resposta das autoridades reguladoras, como a EMA e a Food and Drug Administration [dos Estados Unidos], que encontraram novas formas de avaliação. Estes procedimentos permitiram avaliar de forma paralela e não sequencial os diversos estudos em curso” sobre o desenvolvimento das vacinas contra a Covid-19, sublinhou.
O especialista manifestou-se, porém, esperançado que a “mudança de atitude de muitos governos e organizações”, como a União Europeia, sobre a importância dos sistemas de saúde para o desenvolvimento e bem-estar das populações, “trará benefícios à investigação de novas soluções terapêuticas”.
“A saúde não pode ser considerada só como uma despesa, mas também como um investimento”, concluiu José Aranda da Silva.
Assine o ECO Premium
No momento em que a informação é mais importante do que nunca, apoie o jornalismo independente e rigoroso.
De que forma? Assine o ECO Premium e tenha acesso a notícias exclusivas, à opinião que conta, às reportagens e especiais que mostram o outro lado da história.
Esta assinatura é uma forma de apoiar o ECO e os seus jornalistas. A nossa contrapartida é o jornalismo independente, rigoroso e credível.




Comentários ({{ total }})
Desenvolvimento de antivirais contra a Covid-19 ainda está em fase embrionária
{{ noCommentsLabel }}